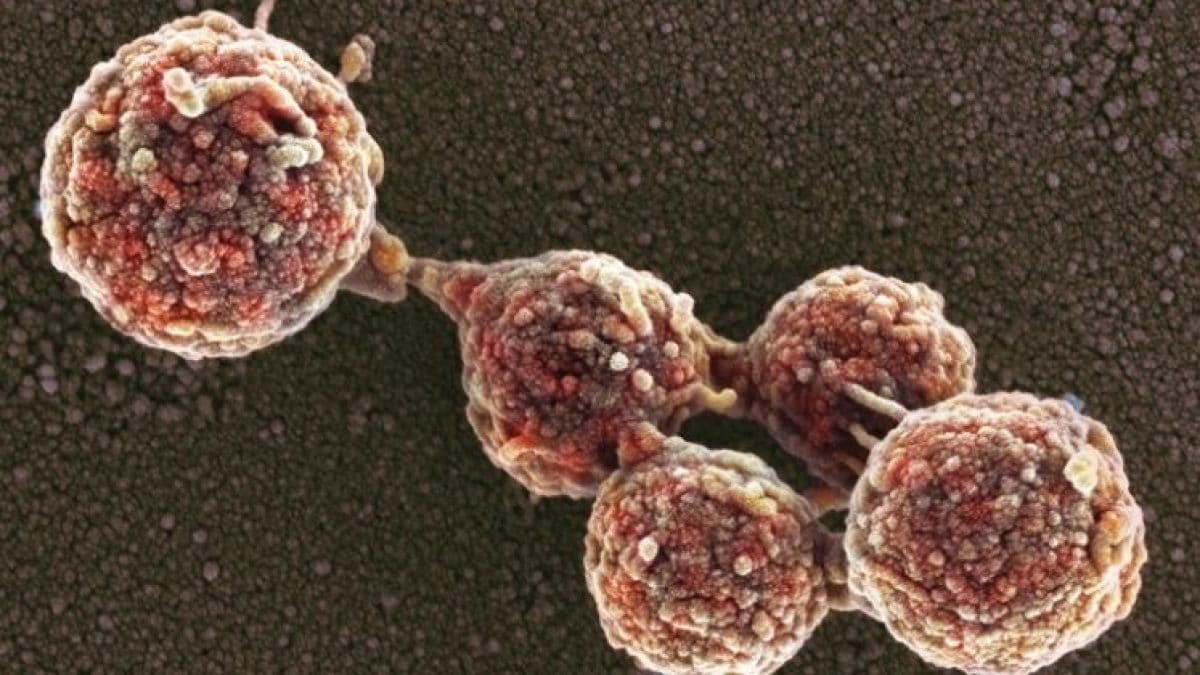
Cellule di batteri ormai morte, con il DNA inattivato, che tornano a vivere dopo aver ricevuto il genoma di un'altra specie. È quanto fatto da un gruppo di ricercatori del J. Craig Venter Institute (JCVI) di La Jolla, California, riportato in un preprint (articolo scientifico non ancora sottoposto a revisione paritaria) pubblicato su bioRxiv a marzo 2026 e commentato dalla rivista Nature. I ricercatori le hanno nominate Zombie cells – cellule zombie – e, nonostante il nome invochi film horror, le loro applicazioni potrebbero aprire nuovi scenari nella biologia sintetica, dalla produzione di farmaci a quella di biocarburanti.
Cos’è il batterio zombie e come funziona
L'esperimento dei ricercatori del J. Craig Venter Institute parte da un problema tecnico che per anni aveva bloccato i ricercatori. Ogni volta che si tentava di trasferire un genoma in una cellula batterica, c'era il rischio di falsi positivi: alcune cellule sopravvivono non perché abbiano davvero "assorbito" il genoma donatore, ma perché il loro DNA originale riesce a incorporare alcuni frammenti di resistenza agli antibiotici attraverso un processo chiamato ricombinazione omologa. Questo rendeva impossibile capire se il trasferimento fosse davvero riuscito.
La soluzione trovata dai ricercatori del JCVI è stata inattivare prima il DNA delle cellule riceventi. Il team ha trattato le cellule del batterio M. capricolum con la mitomicina C, un farmaco chemioterapico che danneggia il DNA. Le cellule così trattate non possono né riprodursi né incorporare frammenti di DNA esterno per ricombinazione. A questo punto, gli è stato "donato" il DNA sintetico di M. mycoides, un batterio di una specie affine ma diversa.
Il risultato è stato che una piccola parte delle cellule "morte" si è risvegliata, riprendendo a crescere e dividersi normalmente, grazie al DNA della specie donatrice. Proprio per questo motivo è stato coniato il termine "cellule zombie". Non per la loro capacità di vagare senza meta alla ricerca di umani da infettare, come accade nei film horror, ma – come spiega Zumra Peksaglam Seidel, biologa sintetica del JCVI e co-autrice dello studio – perché si tratta a tutti gli effetti di «cellule destinate a morire che sono state riportate in vita».
Perché è importante lo studio
Questa ricerca potrebbe aprire la strada a nuove applicazioni in biologia sintetica, la scienza che si occupa di riprogettare gli organismi per scopi utili, ingegnerizzandoli per conferire loro nuove capacità.
Estendere questa tecnica ad altri batteri, compresi quelli più studiati in laboratorio come Escherichia coli, permetterebbe ai ricercatori di testare genomi ingegnerizzati su larga scala. Detto in parole semplici, l'idea sarebbe quella di inserire le "istruzioni" genetiche necessarie per fabbricare queste molecole direttamente all'interno dei microrganismi, trasformandoli in minuscole bio-fabbriche. Oggi un processo simile avviene già, per esempio per la produzione di insulina, ma con la differenza che la tecnica si limita a inserire un singolo gene all'interno del DNA di un batterio vivo e funzionante.
Tuttavia, trattandosi di uno studio non ancora sottoposto alla revisione ufficiale della comunità scientifica, la strada verso queste applicazioni pratiche è ancora lunga e i risultati dovranno essere ulteriormente confermati da esperimenti futuri.
Chi è Craig Venter e cosa ha fatto finora
Per capire il contesto di questa ricerca è importante conoscere l'uomo a cui l'Istituto è intitolato: il biologo e imprenditore John Craig Venter. Nel 2000, nell'ambito del Progetto Genoma Umano, Venter ha sequenziato il DNA in parallelo con il consorzio pubblico internazionale. Successivamente ha fondato il JCVI, con l'obiettivo di studiare le applicazioni della biologia sintetica.
Nel 2010, gli scienziati dell'istituto americano sintetizzarono in laboratorio l'intero genoma di un batterio e lo trasferirono in cellule vive generando quella che i ricercatori chiamarono la prima cellula sintetica della storia (JCVI-syn1.0), un organismo il cui intero patrimonio genetico era stato progettato al computer.
Inoltre, come riporta il National Institute of Standards and Technology (NIST), nel 2021 lo stesso gruppo creò JCVI-syn3A: una cellula con meno di 500 geni (contro i circa 4.000 di Escherichia Coli e i circa 30.000 di una cellula umana) capace di crescere e dividersi normalmente. L'obiettivo era di capire le informazioni fondamentali della vita togliendo tutto il superfluo e lasciando solo l'essenziale.
;Resize,width=767;)

;Resize,width=767;)
;Resize,width=727;)

;Resize,width=727;)
;Resize,width=727;)
;Resize,width=727;)

